利用活性α突触核蛋白构建帕金森动物模型
帕金森是第二大老龄化相关的神经衰退疾病。主要的生物化学改变为神经元中产生不溶性“路易小体”,其主要的成分是聚集的α突触核蛋白。α突触核蛋白在神经衰退类疾病中扮演着重要角色,如路易体痴呆,多系统萎缩症和帕金森,这些疾病统称为突触核蛋白病。在这些疾病中,α突触核蛋白集合形成更大的聚合体,也就是路易体和营养障碍性神经突。α-突触核蛋白是高度易溶的,没有内部结构的小分子蛋白,广泛存在于大脑中,主要分布于神经元突触前体内。α突触核蛋白参与突触小泡的信号分子释放,包括多巴胺,对机体运动非常重要。α突触核蛋白寡聚体(oligomers)具有神经毒性,能以类似朊病毒的方式扩散致病。
α突触核蛋白是一种分子量为14KD的蛋白,主要存在于中脑黑质中的神经元突触前体,目前还不能完全了解其功能。α突触核蛋白的非淀粉样蛋白部分,又称NAC 区域,由中段憎水区构成,是形成蛋白聚集的必要区域。α突触核蛋白单体可以形成各种类型的寡聚体。随着寡聚体形成可溶性原纤维或纤维细丝,蛋白聚集也在持续进行。纤维细丝经过结构变化,从α螺旋结构变成β折叠,然后形成不溶性纤维。这些各种类型的蛋白以动态平衡的形式同时存在。
StressMarq公司是神经衰退疾病研究工具行业的领先制造商,是活性α突触核蛋白单体,寡聚体,前体原纤维的生产商。前体原纤维,又称PFF。PFF是制作帕金森疾病模型的重要工具,它们可以大大加速α突触核蛋白单体的聚集。
在体外通过硫磺素T作为指示剂,当蛋白聚集时形成β折叠时,可以看到增强的荧光信号,这是蛋白聚集的一种固有现象。将PFF加入到原代神经元中或者注射到啮齿动物大脑中,都可造成蛋白聚集和α突触核蛋白病理现象。路易体病理现象从注射点开始蔓延,可用129号位丝氨酸磷酸化的抗体来识别,这是可视化α突触核蛋白病理现象的最佳方法。将 PFF注射到动物脑中制作病理模型,比使用基因改造模型要快10到15倍。该方法制作疾病模型的时间要远远短于传统的基因改造小鼠、大鼠。通常注射后30天即可见到病理反应,而基因改造模型需要9个月到1年时间。为帕金森造模提供了极大的便利。α突触核蛋白PFF还可以结合荧光标记, 用于蛋白示踪。虽然路易体病理现象是突触核蛋白病的最先出现的症状, 但是α突触核蛋白寡聚体在疾病进程中也扮演重要角色,因为它们有很强的神经毒性。α突触核蛋白可以被稳定在寡聚体形式,加入到疾病模型中诱发毒性。
StressMarq的α突触核蛋白产品线包括原纤维,寡聚体和抗体,可以用于研究α突触核蛋白的病理学和毒性特征。这给科研学者提供了有力的工具,用来构建疾病模型,检测新药,一起攻克神经衰退疾病治愈难题。
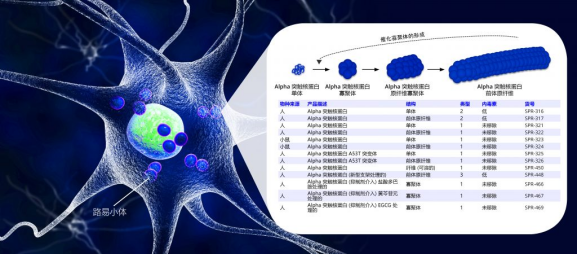
StressMarq目前提供人源和小鼠源前体原纤维(PFFs)以及单体用于帕金森造模的研究。所有蛋白都进行了细胞检测和ThT检测。TEM 图片、ThT检测曲线以及其他检测结果可以在产品单页上看到。A53T α-突触核蛋白单体和PFFs也上线了。A53T突变型被认为与早发型帕金森疾病有关并且加速α-突触核蛋白的纤维聚化。
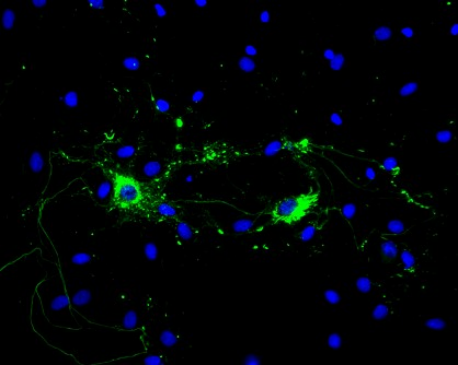
大鼠原代海马神经元经过 1 型 小鼠α-突触核蛋白PFFs处理后显示出路易小体病理现象。
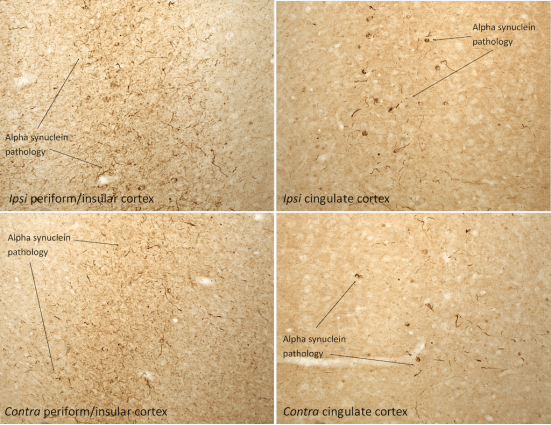
大鼠脑注射了1型小鼠α-突触核蛋白 PFFs (SPR-324) 后的IHC分析,显示了α-突触核蛋白病理现象.
StressMarq目前正在研发更多的原纤维新品用于神经衰退疾病研究,并且也在完善我们现有的产品线。下面表格列出了各种蛋白的区别:
| 1型PFFs(SPR-322) | 1型PFFs(SPR-324) | 1型PFFs(SPR-326) | 2型PFFs(SPR-317) | 3型PFFs(SPR-448) | 蛋白纤维(SPR-450) | |
| 物种来源 | 人 | 小鼠 | 人 | 人 | 人 | 人 |
| 突变类型 | 野生型 | 野生型 | A53T | 野生型 | 野生型 | 野生型 |
| 单体来源 | SPR-321 | SPR-323 | SPR-325 | SPR-316 | SPR-316 | SPR-321 |
| 内毒素水平 | 制作时含有内毒素LPS, 并且没有移除 | 制作时含有内毒素LPS, 并且没有移除 | 制作时含有内毒素LPS, 并且没有移除 | 纤维聚集之前移除了LPS (低内毒素) | 纤维聚集之前移除了LPS (低内毒素) | 制作时含有内毒素LPS, 并且没有移除 |
| ThT 检测 | 与SPR-321 单体混合时荧光强度>12 000 荧光单位 与 SPR-316 单体混合时荧光强度为1300 荧光强度 | 与SPR-323单体混合时荧光强度> 3100 荧光单位 | 与SPR-325单体混合时有28 000 荧光单位 | 与SPR-321单体混合时有3000荧光单位 与SPR-316 单体混合时有400荧光单位 | 调研中 | 调研中 |
| 原代细胞活性 | 在原代大鼠细胞中会诱发路易体病理现象 | 在原代大鼠细胞中会诱发路易体病理现象 | 调研中 | 在原代大鼠细胞中不会诱发路易体病理现象 | 调研中 | 调研中 |
| 活体内活性 | 在大鼠大脑中注射后30天内产生病理反应 | 在大鼠大脑中注射后30天内产生病理反应 | 调研中 | 调研中 | 调研中 | 调研中 |
3型PFFs (使用新型支架制作) 与1 型 PFFs 结构和活性都相似,但是内毒素水平较低与2 型 PFFs 相似。 PFFs 不可溶而蛋白纤维可溶,但是可能根据操作手法不同会有少量不溶原纤维。抑制剂可以停滞alpha突触核蛋白的聚集,阻止寡聚体形成原纤维。以下是抑制剂阻滞的寡聚体:
| 盐酸多巴胺处理的寡聚体 (SPR-466) | 黄芩苷元处理的寡聚体 (SPR-467) | EGCG 处理的寡聚体 (SPR-469) | |
| 抑制剂 | 盐酸多巴胺 (Dopamine HCl) | 黄芩苷元 (Baicalein) | 表没食子儿茶素没食子酸酯 (EGCG) |
| 物种来源 | 人 | 人 | 人 |
| 突变类型 | 野生型 | 野生型 | 野生型 |
| 单体来源 | SPR-321 | SPR-321 | SPR-321 |
| 内毒素 | 制作时含有内毒素LPS, 并且没有移除 | 制作时含有内毒素LPS, 并且没有移除 | 制作时含有内毒素LPS, 并且没有移除 |
只含有抑制剂-阻滞的寡聚体的ThT检测在24小时内没有显示荧光强度增强,当与1型单体混合时荧光强度有所增加。 但是这个增加比单独1型单体的增加要少。这说明这些抑制剂-阻滞的寡聚体减缓了单体的聚集。
ThT是一种荧光染料,可以绑定富含beta折叠的结构, 例如alpha 突触核蛋白原纤维. 抑制剂介入-盐酸多巴胺处理的寡聚体(SPR-466)显示的荧光强度和单体(SPR-321)相比要少得多。单体和抑制剂介入的寡聚体混合后显示的聚集作用很有限。
大鼠活体注射帕金森建模和检测实验
该实验操作指南是将1型小鼠PFFs(SPR-324)或1型人PFFs(SPR-322)注射到大鼠脑中来产生alpha突触核蛋白病理特征。小鼠PFFs显示出了更强的聚集效果。
使用的动物: 雌性 SD(Sprague Dawley) 大鼠
2uLPFFs或者单体 (阴性对照) 通过以下两个脑顶叶区的位置注射:
● AP+1.6,ML+2.4,DV–4.2
● AP–1.4,ML+0.2,DV–2.8
30天后, 用生理盐水灌注大鼠然后在大鼠脑冠状平面切开,将中脑与前脑分开。之后两部分都用4%PFA 固定48小时。
DAB 操作步骤
材料
● 1XTBS (含有和不含有TX-100的)
● 30% H2O2
● 柠檬酸缓冲液
● 驴血清(保存在-20℃;冻融稳定的)
● 一抗:pSYN EP1536Y (Abcam; ab51253)
● 二抗:生物素-SP (long spacer) AffiniPure 驴抗兔 IgG (H+L) (Jackson Immuno; 货号: 711-065-152)
● ABC 试剂 (Vector; 货号: PK-7100)
● DAB 试剂 (Vector; 货号: SK-4100)
● 孔板 (规格取决于要染色的区域数量)
● 漆刷
● 玻璃钩
● 漂白剂
● ddH20
● BD Luer-lock 注射器 10 mL
● 过滤器 0.22 uM 孔径 (Fisher 货号. SLMP025SS)
● 100% EtOH
● Histoclear (用于清理组织)
● 显微镜载玻片和盖玻片
● Permount (封片剂)
第一天:(猝灭, 抗原修复, 阻断, 一抗)
→ 用 1X TBS (震荡, 室温)冲洗切片 5 次以除去冷冻保护剂。
→ 把切片放到 0.6% H2O2 的 TBS 中,覆盖好,置于操作台 20 分钟。
*该步骤不要用 MESH WELLS*
用 _______ mL TBS, _______ uL 30% H2O2
→ 用 1X TBS (震荡, 室温) 冲洗切片 3 次。
→ 做抗原修复时, 提前在水浴中预热柠檬酸缓冲液至少 15~30 分钟。在柠檬酸缓冲液中培养切片一小时,将温度设置为 37℃,不要震荡 。
→ 用 1X TBS (震荡, 室温) 冲洗切片 3 次。
→ 阻断时, 将切片置于 5% 常规驴血清和 0.25% Triton-100 的 TBS 中阻断 1 小时,冷室、震荡。
*注意: 可以使用含有 Triton 的 TBS 阻断液 (1 L TBS, 2.5 mL TX-100), 之后只需要向阻断液中加入驴血清来阻断。*
用 _______ mL TBS,
_______ uL 驴血清, _______ uL 10% TX-100
→ 用 1X TBS (震荡, 室温) 冲洗切片 3 次。
→ 用含 5% 驴血清的 TBS 制备一抗溶液,稀释度为 1:5000。用锡纸包好切片,和抗体一起在冷室中震荡培养过夜。
用 _______ mL TBS,
_______ uL 驴血清, _______ uL pSYN EP1536Y
第二天:(二抗, ABC 扩大信号, DAB 染色)
→ 用 1X TBST (震荡,室温) 冲洗切片 3 次. 余下的步骤中,需要一直将切片保留在锡纸里,即使是冲洗的步骤。
→ 用含 5% 驴血清的 TBS 制备二抗溶液,稀释度为 1:500。在冷室中培锡纸养盖好的切片 2 小时,震荡。
用 ______mL TBS,
______ uL 驴血清, _______ uL 生物素标记的驴抗兔 IgG
→ 用 1X TBST (震荡,室温) 冲洗切片 3 次。
→ 用 ABC 试剂培养切片 30 分钟 (震荡, 冷室)。
→ 用 1X TBS 冲洗切片 3 次 (震荡,室温)。
→ 用 falcon 离心管和 ddH2O 制备 DAB 溶液,每 5 mL H2O 加入如下溶液然后涡旋混合:
2滴缓冲溶液
4滴 DAB 溶液
2滴过氧化氢溶液
*注意: 所有接触过DAB 的器具只能用来操作 DAB。我们还在通风橱内准备了一个 DAB 专用的废液缸。使用玻璃钩来处理 DAB 溶液中的切片而不能用漆刷,并且操作后要用漂白剂冲洗玻璃钩。盛装过 DAB 的器皿都需要用漂白剂冲洗并且处理到生物性危害箱中。*
→ 用注射器过滤到新的6孔板中。每一个需要染色的脑切片都用一个新的 DAB 孔。
→ 在DAB中培养每个切片直到变为浅棕色(2-3分钟就足够; 时间太长可能会造成背景染色太多)
→ 用 ddH2O冲洗3次
→ 在 1X TBS 中封片,然后在切片柜中干燥过夜。
第三天:(脱水和盖玻片)
*注意: 在开始脱水步骤之前,确保浸片用的玻璃皿里有足够的液体可以盖过切片上的所有组织。*
→ 按照如下顺序和时间脱水切片:
1.30秒ddH20
2.3分钟70% EtOH
3.3分钟95% EtOH
4.3分钟95% EtOH
5.3分钟100% EtOH
6.3分钟100% EtOH
*置于振荡器*
7.5分钟 Histoclear
8.5分钟 Histoclear
9.5分钟 Histoclear
→ 将切片从切片篮从取出,一次一片,置于吸水纸上。
→ 加封片剂时,取一个 P1000 移液器和吸头,将吸头尖剪掉,容量设到 400 到 500 μL.
→ 连续滴几滴封片剂 Permount 到切片的中间,倾斜切片使封片剂完全覆盖切片。
→ 用棉棒的木头一端赶出切片中的气泡。
→ 将切片放在吸水纸上,置于操作台上过夜晾干。
*注意: ~24 小时之后, 多余的 Permount 封片剂应该用 Histoclear 移除*
详情请咨询StressMarq全国代理-上海金畔生物科技
